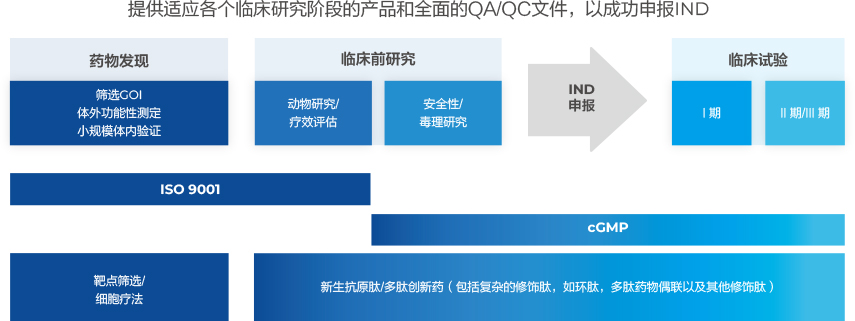
金斯瑞cGMP生產平臺聚焦于提供可靠的一站式服務,涵蓋了早期的多肽藥物開發、IND申報、臨床試驗。我們為客戶量身定制解決方案,滿足客戶的特殊需求。我們專業的藥政事務團隊致力于為多肽藥物的CMC文件和全球監管策略提供全面支持。
20+年專業經驗
cGMP合規性
法規支持

提供滿足IND申報的API生產工藝開發的一站式服務
潔凈區配備A級無菌隔離器,可以提供無菌多肽
提供適用于新生抗原肽的無菌過濾和無菌灌裝服務
提供工藝開發和工藝放大的服務
提供新生抗原肽快速生產、檢測、放行服務,最多每個批次48條個性化新生抗原序列
復雜序列和多種多肽修飾可以提供大規模生產服務,包括環肽和多肽藥物偶聯物。

完整的批生產記錄
質量標準包含鑒別 、純度、微生物限度、內毒素等項目
完善的物料供應商管理體系
分析方法開發、確認、驗證服務
符合ICH要求的長期和加速穩定性測試,強降解研究
完善的質量管理系統: 滿足ICH Q7A和藥品生產質量管理規范
TSE/BSE聲明
金斯瑞專業的生產能力,快速交付能力以及平臺工藝可以為您解決新生抗原肽以及多肽原料藥從早期藥物開發到臨床I/II期的研究。我們的GMP廠房以及一站式服務,可以靈活支持您各個階段的研究項目。